Εξερεύνηση του κόσμου. Μεγάλες ανακαλύψεις. Διαρκής δίψα για κατανόηση. Για εμβάθυνση και γνώση των πάντων. Αυτό είναι ο άνθρωπος. Πέρα όμως από τις εξωστρεφείς ανάγκες του, υπάρχουν και οι εσωστρεφείς. Να βρει που εδράζεται στον εγκέφαλο η κάθε αντίδραση. Να ψαχουλέψει το ίδιο του το υποσυνείδητο. Όλα αυτά βέβαια αφορούν και ικανοποιούν ιδιοτελείς σκοπούς. Ο άνθρωπος έχει την ανάγκη να υπερβεί και να κυριαρχήσει σε πράγματα που μπορεί να μην ταλαιπωρούν τον ίδιο. Τις ασθένειες. Τα κληρονομικά προβλήματα. Τις γονιδιακές ανωμαλίες. Το 2017 και ιδίως το 2018, ίσως είναι οι χρονιές που θα δώσουν τα μεγάλα πλεονεκτήματα στον άνθρωπο σε αυτή την κούρσα απέναντι σε αόρατους εχθρούς. Το δικό του υγρόν πυρ λέγεται Crispr Cas9.
Τι είναι αυτό το Crispr; To Clustered regularly interspaced short palindromic repeats είναι ένας χρωμοσωμικός τόπος στους προκαρυωτικούς οργανισμούς, που περιλαμβάνει μικρές επαναλαμβανόμενες αλληλουχίες βάσεων, οι οποίες τους παρέχουν ένα μηχανισμό άμυνας ενάντια σε βακτηριοφάγους (ιούς των βακτηρίων) και πλασμίδια, προσφέροντάς τους τη δυνατότητα να εξαλείψουν ξένο γενετικό υλικό που εισβάλλει στο κύτταρό τους . Οι επαναλαμβανόμενες αυτές αλληλουχίες ανακαλύφτηκαν αρχικά το 1980 στην Ε.Coli, αλλά η λειτουργία τους έγινε γνωστή το 2007, όταν ο Barrangοu με τους συναδέλφους του μελετώντας τους μηχανισμούς άμυνας του S. Thermophilus, διαπίστωσαν ότι με την εισαγωγή ενός θραύσματος γονιδιώματος ενός ιού στον CRISPR τόπο, το βακτήριο αποκτά ανθεκτικότητα έναντι βακτηριοφάγων.
Πέρα όμως από την προστασία που παρέχει στο ίδιο το βακτήριο, παίζει σημαντικό ρόλο στην τεχνολογία επεξεργασίας του γονιδιώματος, μέσω του συστήματος CRISPR/Cas9 και μπορεί να χρησιμοποιηθεί για να επιφέρει αλλαγές στο γονιδίωμα άλλων οργανισμών.
Το ξένο DNA των πλασμιδίων ή των ιών που εισβάλλει στο βακτηριακό κύτταρο κόβεται σε μικρά κομμάτια και στη συνέχεια εισάγεται στο CRISPR του προκαρυωτικού οργανισμού. Κατά τη μεταγραφή αυτού του τόπου που περιέχει πλέον και κομμάτι ξένου DNA, παράγονται μικρά RNAs, που ονομάζονται crRNAs, τα οποία καθοδηγούν την ενδονουκλεάση Cas9, να κόψει ξένο DNA, που είναι συμπληρωματικό προς το crRNA, δημιουργώντας ρήγματα και στις δύο έλικες του ξένου DNA.
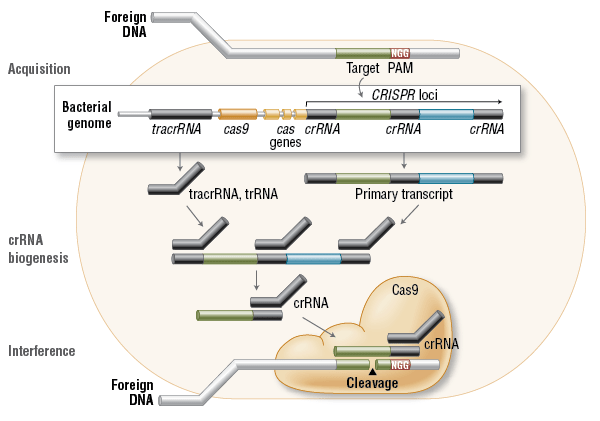
Τι σημαίνει σε πιο απλά λόγια αυτό; Σημαίνει ότι αν για παράδειγμα ένα κύτταρο έχει προσβληθεί από κάποιον ιό, τότε το Crispr Cas9 (που είναι το σύστημα νούμερο 2 σε επίπεδο Crispr) έχει την ικανότητα να πάρει το μολυσμένο σημείο και να το απεμπολήσει. Το ένζυμο Cas9 είναι σαν ένα ψαλίδι που κόβει την διπλή έλικα του DNA του ιού και υποκινεί το κύτταρο, ώστε να γεμίσει το κενό που θα δημιουργηθεί από την αφαίρεση. Αυτή την διαδικασία είναι που θέλουν να απομονώσουν οι επιστήμονες και να την εφαρμόσουν σε μολυσμένα κύτταρα.
Με αυτό τον τρόπο, τα βακτήρια των κυττάρων που θα μείνουν πίσω θα μπορέσουν να αναγνωρίσουν και να αποτρέψουν τον ιό από την είσοδο του. Μέχρι στιγμής η χρήση του Crispr έχει βρει καλές συνθήκες σε επίπεδο γεωργίας, φαρμακευτικής και βιολογικής έρευνας, όπως λέει ο Σαμ Στέρνμπεργκ, επικεφαλής του τμήματος βιοεπιστημών στο Berkeley. Σε αντίθεση με το παρελθόν και το παρόν, όπου οι επιστήμονες χρησιμοποιούν χημικές ουσίες και ραδιενέργεια για να προκαλέσουν γονιδιακές μεταλλάξεις, χωρίς να μπορούν να ξέρουν σε ποιο σημείο του γονιδίου θα έρθει η αλλαγή, το Crispr δίνει ένα μεγάλο πλεονέκτημα. Τη δυνατότητα να γνωρίζουν και να στοχεύουν το σημείο. Τη δυνατότητα να επιταχύνουν την διαδικασία με το χαμηλότερο κόστος. Άνοιξε ένα νέο μονοπάτι σε μια εποχή που τα περισσότερα αντιβιοτικά, όπως αυτά που χορηγούνται σε ασθενείς καρκίνου του προστάτη, δεν μπορούν πλέον να δράσουν. Οι ιοί μετεξελίχθηκαν και η ανθεκτικότητα τους είναι αδιαπέραστη.
Σύμφωνα με τον δρ. Μπγιορν Μπρεντλ, του Universitatsklinikum Schleswig-Holstein της Γερμανίας, το Crispr «μας δίνει την ευκαιρία να δημιουργήσουμε ισογονικά βλαστοκύτταρα. Μετά, να φτιάξουμε ίδια μολυσμένα μοντέλα, με ίδιο γονιδιακό περιεχόμενο. Έτσι θα μπορέσουμε να μελετήσουμε τα μοτίβα και τις διαφορές στα υγιή και τα άρρωστα μοντέλα. Η έκχυση πολυδύναμων βλαστοκυττάρων στους νευρώνες θα αναδείξει και την λειτουργία των φαινοτύπων που μας αφορούν. Στην ουσία πρόκειται για έναν συγκερασμό μηχανολογίας και βιολογίας εντός του κάθε ξεχωριστού γονιδίου».
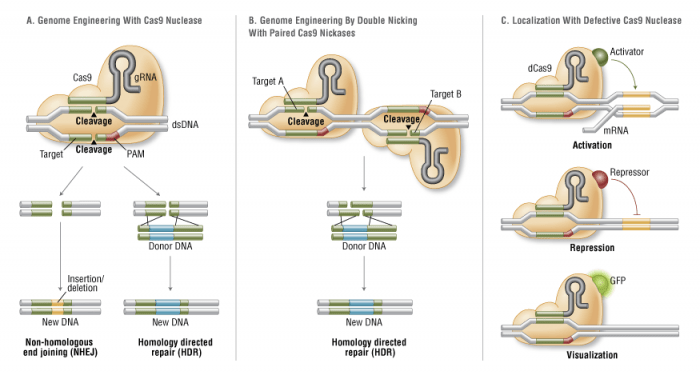
Ο γιατρός Λι Κονγκ και οι συνεργάτες του από την άλλη πέτυχαν μια μετάλλαξη του ενζύμου και το μετέτρεψαν σε Cas9D10A, το οποίο κόβει μόνο ένα νήμα του DNA και δεν ενεργοποιεί τον NHEJ, ένα εργαλείο που επιδιορθώνει τα διπλά νήματα και επιβλέπεις τις εισαγωγές ή αφαιρέσεις. Μεταλλάξεις όπως αυτή δοκιμάζονται με στόχο να αυξηθεί η αποτελεσματικότητα του Cas9, το οποίο βρίσκεται μεταξύ 29 και 50% στην κανονική του μορφή. Στα μέχρι στιγμής πειράματα από τον Κονγκ ή τον καθηγητή Ζάολαν Ζου, η αποδοτικότητα του ενζύμου έχει φτάσει στο 70% σε ένα είδος ψαριού και σε ποικιλίες της χλωρίδας, ενώ σε ένα έμβρυο ποντικιού ανέβηκε στο εντυπωσιακό 78%. Πιο συγκεκριμένα, η επιτυχής εφαρμογή του έχει καταγραφεί μέχρι στιγμής σε: βακτήρια, ζεβρόψαρα, στους μύκητες της ζύμης, στον βάτραχο Xenopus Tropicalis, στα δροσόφιλα έντομα, γουρούνια, μαϊμούδες, λαγούς, αρουραίους, ποντίκια και στον άνθρωπο.
Ποια είναι όμως η εφαρμογή του μηχανισμού; Με τα μέχρι σήμερα δεδομένα, αυτό που μπορεί να ειπωθεί με σιγουριά είναι ότι μέσα από διεργασίες μεταβολής, το Crispr θα έχει την ικανότητα να καταπολεμήσει τον καρκίνο, την ηπατίτιδα Β, την κυστική ίνωση, τη νόσο Lyme, τη νόσο Leber, την μυοκαρδιοπάθεια, την ισχαιμία, το Parkinson και την υψηλή χοληστερόλη.
- Ήδη από το 2016 έχει ξεκινήσει σε 18 καρκινοπαθείς (μελάνωμα, σάρκωμα και μυέλωμα) η θεραπεία με το ένζυμο. Η εισαγωγή του στα άθικτα κύτταρα στοχεύει στην ενίσχυση τους, ώστε να εξαφανίσουν τα καρκινογόνα κύτταρα.
- Το HIV είναι ένας ακόμα δύστροπος και ακατάβλητος ιός. Με τις προβλέψεις πάντως να λένε ότι από το 2030 δεν θα εμφανιστούν νέα κρούσματα, το Crispr έρχεται να δώσει μια επιπλέον ώθηση. Ο Τσεν Λιανγκ, επικεφαλής μιας ομάδας συνεργασίας από το Πανεπιστήμιο του Πίτσμπεργκ και του Temple University, δημοσίευσε τα αποτελέσματα της έρευνας που έκαναν. Σε αυτή την έρευνα βρήκαν ότι τα μολυσμένα κύτταρα των ζώων που εφαρμόστηκε η μέθοδος, έδειξαν τάσεις αποθεραπείας.
- Huntington’s Disease: Η συγκεκριμένη νόσος προκαλεί παράλυση στα νεύρα του εγκεφάλου και η σταδιακή παύση της λειτουργίας τους οδηγεί στο θάνατο. Μια παύση που ξεκινάει από ένα πειραγμένο γονίδιο, το οποίο γιγαντώνεται και γεμίζει με την ουσία χαντινγκτίνη τα διπλανά κύτταρα. Ο Σου Γιανγκ, ερευνητής στο Πανεπιστήμιο Emory της Ατλάντα, δημοσίευσε ένα paper στο Journal of Clinical Investigation, όπου εξηγεί τον τρόπο αντιστροφής της διαδικασίας της νόσου. Με τη χρήση του Crispr στα κύτταρα ποντικών, πέτυχαν να αναστρέψουν την παράλυση. Οι νευρώνες που είχαν μολυνθεί δεν μπορούσαν να μολύνουν τους όμορους και άρχισαν να επουλώνονται.
- Παρέμβαση στο DNA του εμβρύου. Προσπαθώντας να μην ξεπεράσουν την γραμμή της ηθικής, οι επιστήμονες στο The National Academies of Sciences, Engineering and Medicine εξέτασαν σε θεωρητικό πλαίσιο τη χρήση του Crispr σε έμβρυα. Μόνος στόχος να πειράξουν τη γονιδιακή τους σύσταση, εφόσον παρουσιάσει το έμβρυο ανωμαλίες. Κάτι τέτοιο είναι το πιο δύσκολο στην πράξη, γι΄αυτό και θα αργήσει περισσότερο από κάθε άλλη χρήση του ενζύμου.
Το πρόβλημα στο παρόν και το μέλλον της βιοϊατρικής-βιοηθικής
Φυσικά, στην ως τώρα προσπάθεια της επιστημονικής κοινότητας ανθίσταται ένα ζήτημα πρακτικής και ηθικής. Ο λόγος είναι ότι η παρέμβαση στα γεννητικά κύτταρα αποτελεί σημείο διαφωνίας. Ενώ τα σωματικά κύτταρα δεν υψώνουν ηθικολογίες, τα γεννητικά δεν επιτρέπουν μονοκόμματες αποφάσεις. Αυτό συμβαίνει γιατί η όποια παρέμβαση σε αυτά, καθορίζει το DNA της επόμενης γενιάς. Αν γίνει σε έναν ανθρώπινο οργανισμό, τότε οι απόγονοι του θα πάρουν το γονιδιακό αποτύπωμα του. Η παρέμβαση στο DNA μπορεί να μετατρέψει την ιατρική σε μηχανή μαζικής παραγωγής. Όλοι θα θέλουν τα παιδιά τους να αποκτήσουν γονίδια ομορφιάς και ευφυΐας λόγου χάρη.
Μια τέτοια δύναμη είναι μη διαχειρίσιμη σε ανθρώπινα χέρια. Ιδίως σε χέρια ανθρώπων που μπορεί να βρεθούν στο δίλημμα επιτήδειων κυβερνήσεων ή των λόμπι. Έχει ξανασυμβεί στο παρελθόν, συμβαίνει και σήμερα. Μπροστά στις ανακαλύψεις που εξαλείφουν ένα πρόβλημα, ορθώνονται οικονομικά συμφέροντα.
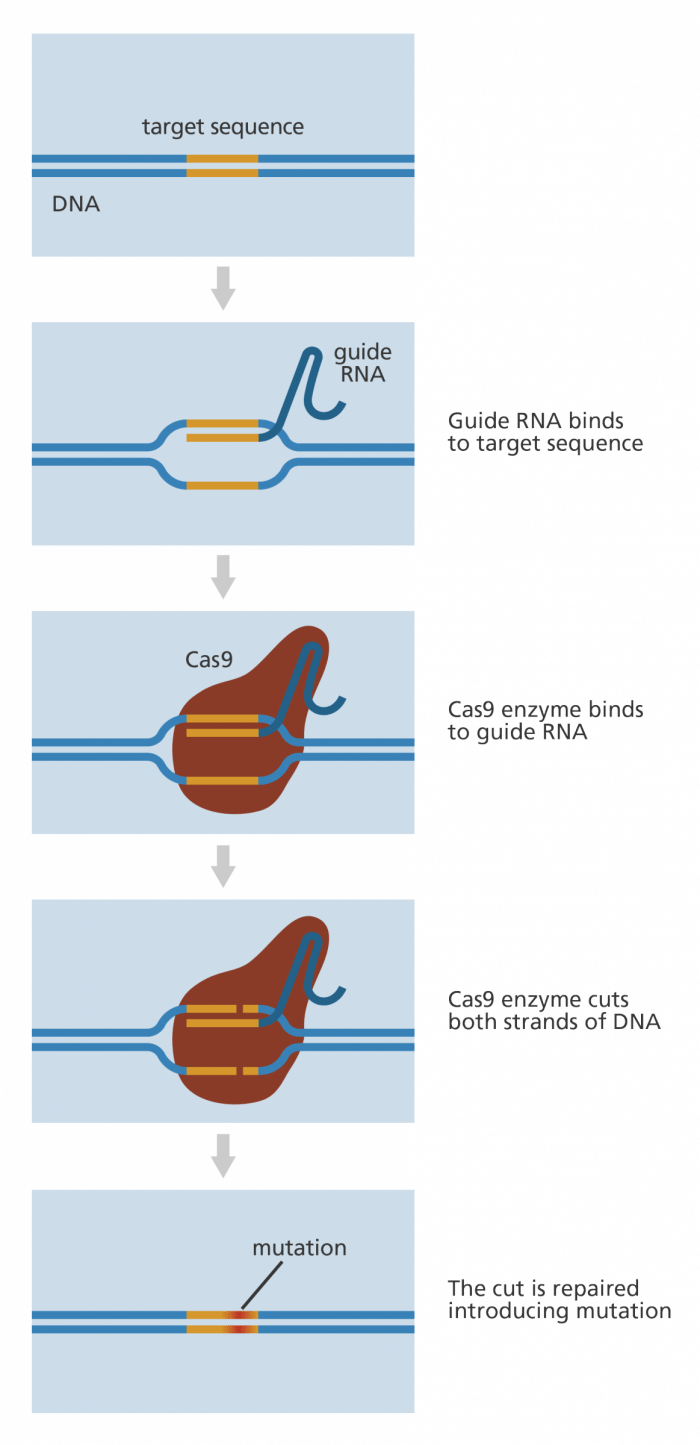
Το παραπάνω καθιστά την ευρεία χρήση του Crispr Cas9 αρκετά μακρινή περίπτωση. Η επόμενη δεκαετία πιθανότατα θα παραμείνει διάστημα πειραματισμών. Ένα διάστημα που ορίζει ο Νέβιλ Σαντζάνα, βιολόγος στο New York Genome Center και επίκουρος στο Πανεπιστήμιο της Νέας Υόρκης. Χωρίς αυτό να αναιρεί το γεγονός ότι μέσα στους επόμενους 14-18 μήνες θα ξεκαθαρίσουν πολλά πράγματα. Άμεση στόχευση προς το βραχυπρόθεσμο μέλλον είναι ο οδηγός RNA. Η αλυσίδα 20 βάσεων που διαθέτει θα πρέπει να ταιριάξει με την αλυσίδα του DNA του γονιδίου που έχει τεθεί σε διαδικασία προσθαφαιρέσεων. Δεν είναι απαραίτητο το 20/20. Η βάση που έχει τεθεί είναι το 15/20 για αρχή.
Η δεύτερη και εγγενής δυσκολία που εντοπίζεται εδώ είναι η εξής. Αν το οποιοδήποτε ματσάρισμα με το RNA γονιδίωμα βρίσκεται και σε άλλο κύτταρο, το RNA μπορεί να αποπροσανατολιστεί και να πάει να κολλήσει σε «καθαρό» κύτταρο.
Επομένως, η μεγάλη πρόκληση που έχει μπροστά της όλος ο κλάδος είναι η μελέτη όλων των κοντινών προς το επίμαχο γονιδιωμάτων, με σκοπό να σιγουρέψουν ότι το RNA δεν θα έχει επαφή με παρεμφερείς συνέχειες. Σε δεύτερο στάδιο η παρουσία ενός συμπλέγματος. Αυτό θα αποτελείται από δύο Cas9 ένζυμα και δύο RNA οδηγούς. Έτσι, ακόμα κι αν ο ένας οδηγός μπερδευτεί και καταλήξει σε άλλο κύτταρο, θα υπάρχει ο άλλος για να αναπληρώσει.
Με δύο μεγάλες εταιρείες στον τομέα της βιοϊατρικής, τις Nemesis Bioscience και Eligo Bioscience να αναπτύσσουν στα εργαστήρια τους αντιμικροβιακές τεχνολογίες και θεραπείες βασισμένες στο Crispr Cas9, τότε μπορούμε να ελπίζουμε σε ένα μέλλον που η υγεία σε επίπεδο ανίατων σήμερα νόσων, θα είναι ένα κεκτημένο!
Πηγή: www.livescience.com, www.technologynetworks.com, www.neb.com, www.yourgenome.org,

